GS1 China 中國物品編碼中心是國家藥監局指定發碼機構,官方發碼,UDI編碼賦碼合規無憂!
企業開通GS1 UDI服務平臺,可實現在一個平臺完成從廠商識別代碼申請、UDI編碼、備案至中國商品信息服務平臺及藥監局數據庫、信息管理、標簽設計、打印噴碼等UDI實施全流程。
目前已實施UDI的醫械企業,90%以上采用GS1碼制,如果你的企業也遇到UDI實施問題,如果你的企業也遇到UDI實施問題可以看下圖,了解GS1一站式UDI服務。
一、UDI法規基礎介紹
中國UDI的“基本法”是《醫療器械唯一標識系統規則》,這個規則是2019年8月發布的。其基本目的是為了貫徹落實《國務院辦公廳關于印發治理高值醫用耗材改革方案的通知》(國辦發〔2019〕37號),規范醫療器械唯一標識系統建設,加強醫療器械全生命周期管理。
首先回顧一下中國醫療器械UDI實施的一些關鍵時間點:
2019年7月 ——【藥監綜械注〔2019〕56號】 關于印發醫療器械唯一標識系統試點工作方案的通知: 拉開了中國UDI的序幕 ;
2019年8月 ——【2019年第66號】國家藥監局關于發布醫療器械唯一標識系統規則的公告: 中國UDI的規則被正式建立 ;
2019年10月 ——【2019年第72號】國家藥監局關于做好第一批實施醫療器械唯一標識工作有關事項的通告:明確了第一批實施產品及其時間點;
2019年12月 —— UDI數據庫正式上線 ;
2020年9月 ——【2020年第106號】關于深入推進試點做好第一批實施醫療器械唯一標識工作的公告: 第一批實施產品時間點推遲到2021年1月1日 。
二、什么是UDI?
唯一器械標識(Unique Device Identification,縮寫UDI), 醫療器械唯一標識是指呈現在醫療器械產品或者包裝上的由數字、字母或者符號組成的代碼,用于對醫療器械進行唯一性識別。
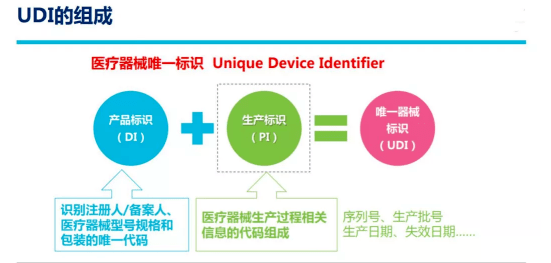
UDI可以被看作醫療器械產品在供應鏈中的唯一“身份證”, 應包括產品標識和生產標識。產品標識為識別注冊人/備案人、醫療器械型號規格和包裝的唯一代碼;生產標識由醫療器械生產過程相關信息的代碼組成,根據監管和實際應用需求,可包含醫療器械序列號、生產批號、生產日期、失效日期等。
三、什么是UDI數據載體?
UDI數據載體 ,是 指存儲或者傳輸醫療器械唯一標識的數據媒介 , 其應當滿足自動識別和數據采集技術以及人工識讀的要求,通俗來說就要包括兩部分:一部分是 機器可讀 ,其形式可以為 一維碼、二維碼或者射頻標簽 ;另外一部分是 人工可讀 ,即應為數字和/或字母的形式。
四、什么是UDI數據庫?
UDI數據庫 ,是 指儲存 醫療器械唯一標識的 產品標識 與 關聯信息 的 數據庫 。與美國的GUDID系統和歐盟的UDI數據庫類似,該數據庫對公眾開放,供公眾查詢。藥監局負責建立及維護該數據庫; 注冊人 /備案人 應在產品上市銷售前,將產品標識(DI)及相關數據上傳至該數據庫 ,并 維護更新相關數據 。
五、發碼機構是什么?中國有哪些認可的發碼機構?
器械唯一標識的發碼機構應當為 中國境內的法人機構 ,具備完善的管理制度和運行體系,確保按照其標準創建的醫療器械唯一標識的唯一性,并符合我國數據安全有關要求。
發碼機構應當向注冊人/備案人提供執行其標準的流程并指導實施,為便于注冊人/備案人等掌握發碼機構的編碼標準,供相關方選擇或應用,發碼機構應當將其編碼標準上傳至醫療器械唯一標識數據庫并動態維護。
目前中國認可的發碼機構有三家:
六、UDI實施準備
熟悉UDI的基本法《規則》、持續跟蹤UDI的相關法規:
就目前來說,監管部門只公布了第一批UDI實施目錄和實施時間,當前目錄中涵蓋的是III類高風險器械,包括:有源手術器械、無源手術器械、神經和心血管手術器械、醫用成像器械、輸血、透析和體外循環器械、有源植入器械、無源植入器械、注輸、護理和防護器械、眼科器械等共9大類產品,具體產品類別見國家藥監局/國家衛生健康委/國家醫保局公告(2020年 第106號),實施時間為2021年1月1日。
熟悉UDI相關標準:
與UDI相關的標準,主要包括:
選擇合適的發碼機構:
如果只考慮中國市場,我們可以選擇前文中三家發碼機構中的任何一家。但由于不少器械的銷售市場不僅僅局限于國內。在這種情況下,我們發碼機構的選擇就要兼顧到海外監管部門的要求(美國、歐盟)。
下表是目前歐盟和美國監管部門認可的發碼機構。
由此我們可以看出,只有GS1一家機構能同時滿足中國、歐盟和美國的要求。(下文如果沒有特別說明,就以GS1來舉例)
申請注冊人備案人識別代碼
注冊人備案人識別代碼通常有7~10位數字組成,這個代碼可追溯到某個特定注冊人備案人。注冊人備案人代碼前三位是前綴碼,國際物品編碼協會已經分配給中國GS1的前綴碼為690-699。我們在申請的時候可以參考GS1的官網,在GS1的官網上面給了比較清楚的步驟,如下:
確定UDI的組成:
我們之前已經了解到:醫療器械唯一標識包括產品標識和生產標識, 即UDI=產品標識(DI)+生產標識(PI)。
UDI的結構示意圖如下(摘自YY/T 1630-2018 附錄A):
上面的產品標識和生產標示只是一個示意圖,DI和PI可以是串聯,也可以并聯的。下面是兩個不同廠家的UDI示例,供參考。
UDI規則和GS1的標準的對應關系如下:
產品標識UDI-DI:
UDI-DI是一個靜態信息,用來指明供應鏈中某個醫療器械的身份信息。在中國,GB 12904中規定了商品條碼即GTIN的表示方法。對于醫療器械,最常見的表示方法為GTIN-14,下面我們就以GTIN-14來舉例:
上圖GTIN-14的第一位(D1)為指示位(indicator),用來指示不同的包裝等級;剩下的第2到第13位(D2 - D13)分別包括注冊人備案人識別代碼、商品項目代碼;最后一位(D14)為校驗碼。
注冊人備案人 識別代碼 由7-10位數字組成,由中國編碼中心負責分配和管理。注冊人備案人識別的前3位為前綴碼,前綴碼由國際物品編碼協會分配給中國。
商品代碼由5-2位數字組成,一般注冊人備案人可自行編制。
校驗碼有1位數字,用于檢驗整個編碼的正誤。校驗碼可以自行計算,其方法可以參考標準GB12904-2008的附錄B。從實操角度來說,目前很多編碼軟件能自動計算產生。
生產標識 UDI-PI:
UDI-PI對應于GS1標準來講即為應用標識符。它是一個動態信息,其內容通常為序列號、批號、生產日期和有效期(失效日期)等;它屬于某個特定醫療器械的動態附加信息,可以跟蹤到具體的產品或者批次。
根據《GB/T 16986-2018 商品條碼 應用標識符 》,應用標識符常見格式如下:
建議醫療器械廠家根據自己的實際情況(以滿足追溯的要求)來確定產品的生產標識信息。例如:
1、對于要求追溯到批次的器械,由DI聯合PI中的生產日期/有效期、批號實現。
2、對于要求追溯到單品的醫療器械,由DI聯合PI中的生產日期/有效期、序列號實現。
七、UDI標簽生成
在產品完成GTIN(UDI-DI)分配,同時確定了產品的生產標識 UDI-PI后,下一步的動作就是生成UDI標簽。按照中國法規的要求,UDI應包括兩個部分:
(1)機器可讀碼,目前最為常見的形式就是一維碼和(或)二維碼。(注冊人備案人可以根據自己的產品實際情況選擇合適的UDI載體)。
(2)人工可讀,即為數字和字母組合。
怎么產生一維碼、二維碼?現在市面上有很多現成軟件能自動產生一維碼、二維碼,也有很多這方面的廠家提供服務,可以基于自己的實際情況去選擇適合自己的方法。
在生成完一維碼、二維碼后,注冊人備案人需要對現有標簽進行標簽變更。之后就可以完成UDI標簽打印及UDI標簽的檢驗,標簽檢驗的目的就是保證UDI可以在整個流通領域的可讀性。
在完成上面的動作后,我們是否就能滿足中國UDI的要求?是否就能把UDI標簽貼在產品上去上市流通了呢?當然不是。
八、UDI數據上傳
產品要上市流通,還要完成下面的環節 :
(1)注冊人備案人應當 在申請醫療器械注冊 、 注冊變更或者辦理備案時 , 在注冊/備案管理系統中提交其產品標識 (UDI-DI)。注意:產品在UDI實施日前,已生產銷售的醫療器械可不具備醫療器械唯一(UDI)標識。
(2)注冊人備案人在銷售產品之前 ,應確保產品標識和相關數據上傳至中國醫療器械唯一標識數據庫(UDID) 。 同樣的這也是針對已經實施UDI的產品,對尚未列入實施目錄的產品不強制要求。
相關數據是什么 ?相關數據包括哪些內容?請參考標準《YY/T 1752-2020 醫療器械唯一標識數據庫基本數據集》。里面對于每個數據集都有相關的解釋。
怎么填報呢 ?請參考標準《YY/T 1753-2020 醫療器械唯一標識數據庫填報指南》。具體操作可以通過國家藥品監督管理局網上辦事大廳實現系統登錄操作。
完成以上的動作,可以認為該醫療器械已經能滿足中國UDI的最基本要求。
最后,建議注冊人備案人 建立相關的程序文件來確保整個過程是是受控的 、 可持續的,使UDI管理過程規范化、制度化。
01
UDI是什么?
UDI(Unique Device Identification)又叫醫療器械唯一標識,是一串由符號、數字或者字母組成的代碼,一般附著在醫療器械產品和包裝上。它是醫療器械唯一標識系統中最重要的一環,具備全球唯一性,可用于醫療器械產品的精準識別,便于監管和追溯,所以也被稱為醫療器械產品的“數字身份證”。
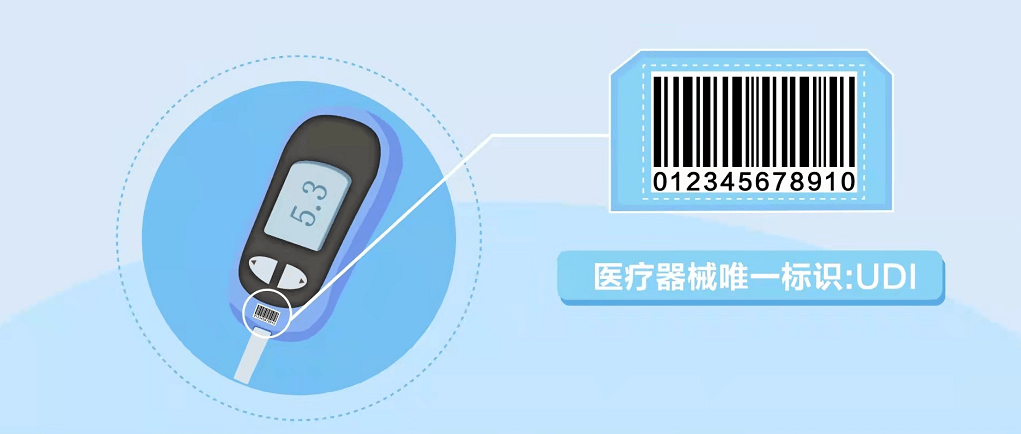
UDI存在于醫療器械產品生產、流通、使用的整個生命周期中,是精準識別醫療器械信息的基礎。由產品標識(DI)和生產標識(PI)兩部分組成。DI是產品靜態信息,包括企業編碼和產品ID。其中,企業編碼由備案人申請,由符合我國醫療器械編碼規則和標準的發碼機構發出的,是具備唯一性的編碼;產品ID是一段包含具體產品名稱、包裝等級、規格型號的編碼。PI是產品動態信息,包括生產日期、失效日期、生產批次、序列號、校檢位等。目前,PI編碼暫不需要上傳到藥監局數據庫,各使用單位可采用掃描設備直接獲取產品相關生產信息。
數據載體、UDI和數據庫共同組成了UDI系統,它可以提高醫療器械不良事件報告的質量,更有效地識別產品問題,更迅速地召回問題器械,以確保患者的安全。

推行UDI的過程
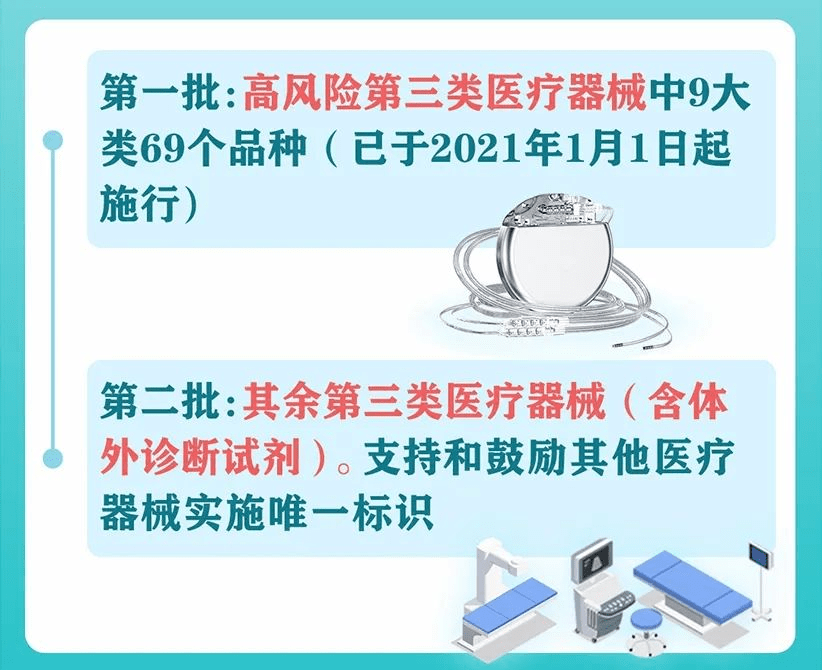
早在1999年開始,UDI相繼在美國、歐盟和日本等國家和地區得到了積極推進。而我國,于2021年1月1日起,高風險第三類醫療器械中9大類69個品種作為第一批開始施行,其余第三類醫療器械(含體外診斷試劑),支持和鼓勵其他醫療器械實施唯一標識。到今年6月1日起,醫療器械就全面進入UDI時代了。距離明確的時間節點,已經迫在眉睫。

02
推行UDI有什么意義?
UDI存在于醫療器械產品生產、流通、使用的整個生命周期中,是精準識別醫療器械信息的基礎。
01
對于企業來說
建立UDI系統有助于提升企業信息化管理水平,建立產品追溯體系,提升企業管理效能,助推醫療器械產業高質量發展。
02
對于流通機構來說
建立UDI系統有助于流通企業建立現代化物流體系,實現醫療器械供應鏈的透明化、可視化、智能化。
03
對于醫療機構來說
建立UDI系統有助于加強醫療器械在臨床使用環節的風險管控,降低器械使用差錯,保障患者用械安全;
04
對于監管部門來說
建立UDI系統有助于醫療器械監管部門構建器械監管大數據,實現對醫療器械來源可查、去向可追,責任可究,實現智慧監管。
05
對于社會相關部門來說
建立UDI系統有助于提升衛生、醫保、海關等部門,對于醫療器械臨床使用、招標采購、醫保結算,進口通關等環節的管理效率;
06
對于廣大用械者來說
有助于放心用械、明白消費。
UDI系統將推動實現醫療器械智慧監管與社會共治,助力產業轉型升級和健康發展,為公眾提供更加安全高效的醫療服務,增強人民群眾的獲得感、幸福感和安全感。

03
UDI如何實施落地?
法治理念根植于一定社會的經濟、政治、文化等諸方面必然性要求之中,它是法治的靈魂,體現了法治的精神實質和價值追求,所要解決的是為什么實行法治以及如何實現法治的問題。
無論是政策,還是從施行的意義上,建立UDI系統已成為每個醫療器械企業必須完成的事項。那么如何開展相關工作,迅速落地實施呢?
01
申請廠商識別代碼
企業需到中國物品編碼中心申請9位廠商識別代碼。
02
綁定UDI管理系統及授權
企業需到國家藥品監督管理總局申請綁定“醫療器械唯一標識管理系統”,并授權第三方編碼機構作為產品唯一標識數據接口。
03
UDI編碼、賦碼
開通第三方編碼機構后,錄入DI和PI信息,建立專屬UDI系統。
然而,在真正落地執行的過程中,不少器械企業卻遇到了諸多困難,如:
(1)UDI編碼規則到底是什么?怎樣才能合法合規?
(2)已有的生產線是否需要更換生產設備?花費成本大嗎?
(3)識別設備系統不兼容,維護困難
……
研發設計醫療器械如此艱巨的任務都已完成,難不成要被這個小小的UDI阻難前進的步伐?放心,無限云溯作為提供醫療器械UDI系統一站式解決方案的提供商,擁有縝密的溯源系統,助力醫療器械企業一舉搶占市場先機。
無限云溯累計發明專利及知識產權高達70多項,其中發明專利18項,軟件著作權50余項。先后獲得了“國家高新技術企業”、“雙軟企業”、并成功通過CMMI三級和ISO90012008質量管理體系認證。可以做到:
01
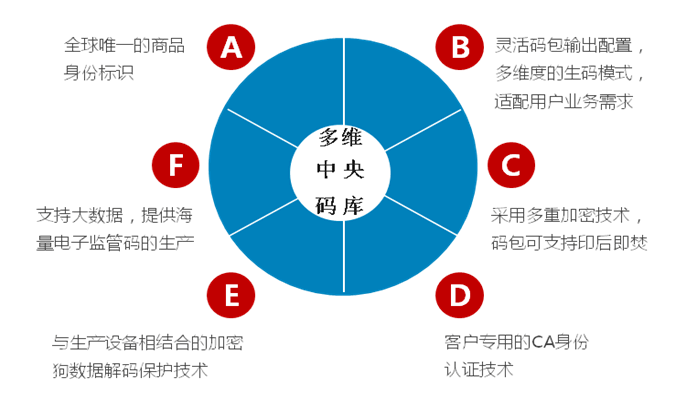
多維中央碼庫,滿足醫療器械全場景賦碼需求
可以通過無限云溯系統的靈活配置,生成多維度組合方式的一物一碼的具有電子監管碼特性的數據碼包,并應用到智能包裝印刷或是電子標簽(RFID)的賦碼環節,以滿足不同應用場景的企業生碼和賦碼的需求。
多維度既包括單一的電子監管碼的生成,也包括電子監管碼+驗證碼、電子監管碼+驗證碼+序列號的組合方式,還支持多層級具有包裝關聯屬性的套標碼的生成,以及具有圖形視覺效果的二維碼的生成等電子監管碼的輸出方式,多維度的滿足醫療器械企業的賦碼需求,基于商品的數字包裝、智能包裝、電子標簽的感知標識的實現。
02
全環節信息采集,保障信息真實有效
提供移動設備PDA的標準化產品,通過業務日常操作,完成器械信息數據的采集。可支持器械的生產數據采集、品質信息采集、出入庫信息采集、零售終端信息采集和消費者的行為數據采集,通過器械的包裝印刷、生產、流通、零售等作業環節的數據采集,收集企業的大數據,為后續各類應用提供原始數據支撐。
通過作業環節的數據采集,用戶可以很靈活的選擇電子監管碼的激活,確保被激活的電子監管碼是真實有效,避免了碼值有效性的外泄風險。

03
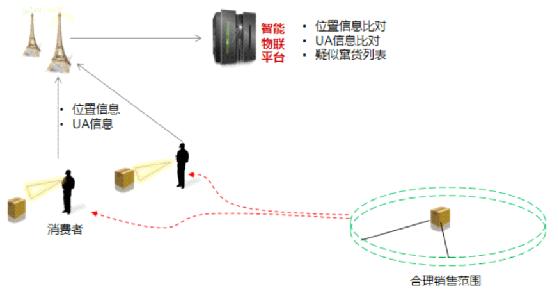
全方位追蹤信息,防止醫療器械竄貨
為管理市場秩序和產品質量,防止產品亂價,企業往往需要通過追蹤了解產品在各個區域銷售狀態,加強對產品數據管理,監督每批產品去向,完成竄貨預防。
無限云溯可依據多維中央碼庫的生碼,在經銷商、用械者掃碼過程時,系統將實時采集地理位置信息,將采集到的地理信息與商品分揀時關聯的經銷商銷售區域信息進行對比,實施竄貨監控及預警,讓防竄貨稽查工作有的放矢。
04
數據共創共享,提供可靠信息
通過建立起來的信息系統,把采集到的UDI數據,通過多種方式將數據共享給經營企業、醫療機構、政府相關部門及社會公眾。為相關部門的監管、追溯、預警、召回、企業的投資、經營管理提供可靠數據依據。

醫療器械UDI,作為解決醫療器械全球監管問題的通用語言、國際語言和專業語言,是實現我國醫療器械全球化、信息化數字化產業發展的必然之路,是提高監管和社會治理能力的有效手段,更是中國器械走向世界的現實要求。





