UDI是什么意思?
醫療器械唯一標識(Unique Device Identification,簡稱UDI)由產品標識和生產標識組成,能夠為每個醫療器械產品賦予唯一的“數字身份證”,實現生產、經營、使用各環節的透明化、可視化,提升產品的可追溯性,是醫療器械監管手段創新和監管效能提升的重要抓手,對確保公眾用械安全有著積極且重要的意義。
根據相關要求,2022年6月1日起生產的第三類醫療器械,應當具有醫療器械唯一標識。

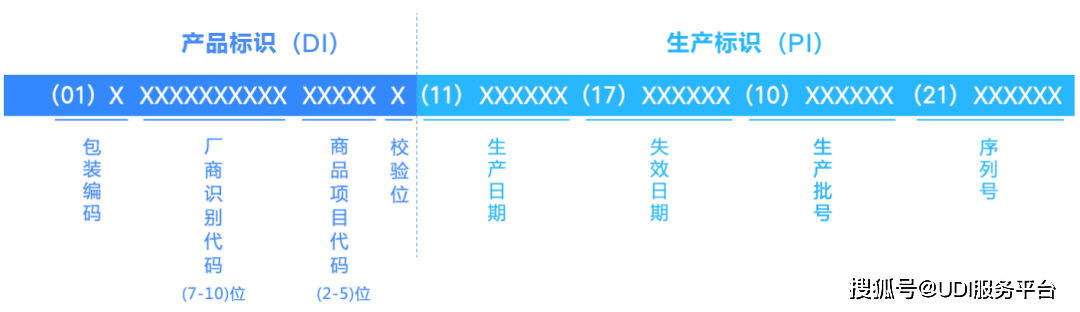
UDI系統由UDI識別符、UDID數據庫和AIDC數據載體構成。UDI識別符由DI 和PI 兩部分組成。
產品標識(DI)
產品標識屬于靜態信息,是器械產品的身份標識,包括識別注冊人/備案人、醫療器械型號規格和包裝的唯一代碼。
生產標識(PI)
生產標識屬于動態信息,用于標識醫療器械產品的生產信息,包括序列號、批號、生產日期和有效期等,其與DI聯合使用才能指向特定的醫療器械產品。
醫療器械唯一標識管理信息系統(UDID)
醫療器械唯一標識數據庫“UDID”由國家藥品監督管理局組織建立,并制定醫療器械唯一標識數據相關標準及規范,以供公眾查詢。醫療器械唯一標識管理信息系統主要用于醫療器械產品標識(UDI-DI)及相關信息的申報管理,具有UDI-DI維護、變更、管理等功能。
AIDC數據載體
UDI數據載體是存儲和(或)傳輸醫療器械唯一標識的數據媒介。器械UDI載體應當滿足機器識別(AIDC)和人眼可讀(HRI)的要求,可采用一維條碼、二維條碼或者RFID電子標簽等形式。
根據國家藥監局制定的《醫療器械唯一標識系統規則》(以下簡稱《規則》)要求:
注冊人/備案人應當在申請醫療器械注冊、注冊變更或者辦理備案時,在注冊/備案管理系統中提交其產品標識。
注冊人/備案人應當在產品上市銷售前,將產品標識和相關數據上傳至醫療器械唯一標識數據庫。

UDI為何如此重要?
減少醫療差錯;簡化將器械使用信息集成到數據系統的操作,識別出現不良事件的醫療器械;更加迅速地為已報告的問題制定解決方案,實現重點突出且有效的安全溝通;安全訪問明確器械標識信息的原始來源。

UDI DI 編碼分配原則
1.根據監管部門的要求,優先分配代碼;
2.根據代碼發布機構的標準和規范分配代碼;
3.唯一性原則:同一規格型號的產品原則上應賦予一個最小銷售單位產品標識,不同規格型號的產品應賦予不同的產品標識,同一規格型號不同產地的產品可賦予不同的產品標識;不同的產品標識應賦予不同的包裝規格;
4.一般來說,產品的基本特征包括產品名稱、商標、類型、規格、數量和包裝類型等產品特征。醫療器械注冊人/備案人可以根據產品特點和自身產品管理需求,為產品分配唯一的DI;
5.如果最小銷售單位包含一個以上使用單位相同的產品,產品標識應分配給使用單位;
6.穩定性原則:DI一經分配,如果產品的基本特性沒有改變,則應保持不變;
7.對于以下情況,需要分配新DI:
1)當監管部門或醫療器械唯一標識數據庫有新的或明確的管理要求時,應分配新的DI;
2)代碼發布機構的標準和規范有新的要求,需要分配新的DI;
3)產品注冊備案時,當上報的某一特征信息發生變化,需要分配新的DI,可能影響使用安全和臨床應用,或可能導致安全性和風險管理的模糊性;
4)當產品注冊和備案時,如果構成產品貿易項目特征的任何報告要素發生變化,應分配新的DI。
8.重新使用DI代碼
1)醫療器械注冊人/申報人必須確保分配給受監管醫療器械產品的DI代碼永遠不會被重復使用。
2)例外情況:對于已經退出市場、重新上市銷售和處于監管之下的醫療器械產品,如果必須申請新的DI代碼,而沒有DI分配規則中提到的任何具體變化或修改,則原DI代碼可用于該產品。舉個例子,生產商從市場上撤回了“產品A”的第一代體外診斷試劑。在缺席市場10年后,廠商按照原來的形態和包裝配置重新推出了“A產品”。在這種情況下,產品可以使用原始DI代碼。
9.包類/組套類產品,DI分配遵循原則:
1)對于包/套產品,如果包/套共同完成一個預期的臨床使用,阿迪將被分配到該包/套產品(如麻醉包);
2)醫療器械注冊人/備案人應當考慮對使用者的安全使用負責(如將DI作為一個整體進行標記,不得拆分運輸,避免使用過程中組裝搭配錯誤);
3)如果包裝/套裝中的產品是獨立的醫療器械產品,可以分配DI;(單獨銷售/使用的情況)
4)對于包/套內非獨立的醫療器械產品(已認定為醫療器械管理的除外),根據內控和質量體系管理的需要,可采用UDI管理,但數據無需上報





